Introducción a la electroquímica:
Introducción a la electroforesis horizontal
Junto con la temperatura y la masa, el pH es la medida más común en los laboratorios. Toca muchos campos, como el análisis de las aguas o aguas residuales, la investigación y el desarrollo más básicos, las ciencias medioambientales, químicas y de la vida, así como a un sinfín de aplicaciones industriales.
A continuación se muestran algunos ejemplos del pH en los productos industriales y domésticos comunes:
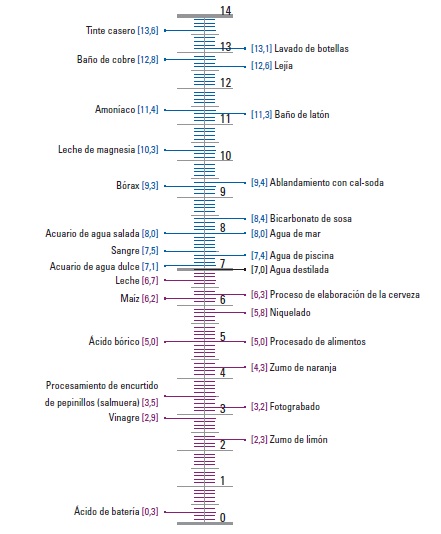
El pH resulta el método más cómodo para comparar la acidez o alcalinidad relativa de una solución a una temperatura determinada. El propio término «pH» es el resultado de una combinación de las letras «p», procedente de la palabra «poder», y «H», que representa el símbolo del elemento hidrógeno. Juntas, significan «el poder del hidrógeno».
Por lo tanto, el pH es el grado de acidez o de alcalinidad de una solución basada en la actividad del ion hidrógeno, representado por la ecuación:
pH = -log [H+]
Expresado matemáticamente, el pH es el valor logarítmico negativo del ion hidrógeno. Dado que están basadas en una escala logarítmica, cada unidad de pH representa un factor de 10, por lo que una solución con un pH de 5 es 100 veces más ácida que un pH de 7.
El pH se mide en una escala que varía de 1 a 14, siendo 1 muy ácido, 14 muy alcalino y 7 neutro. Un pH de 7 describe una solución neutra porque las actividades de los iones de hidrógeno e hidróxido son iguales. Cuando el pH es inferior a 7, la solución se describe como ácida porque la actividad del ion de hidrógeno es mayor que el del ion hidróxido y, como la actividad del ion hidrógeno aumenta, el valor de pH disminuye. Por el contrario, cuando el pH es superior a 7, la solución se describe como básica (o alcalina), porque la actividad del ion de hidróxido es mayor que la del ion de hidrógeno.
El pH puede medirse de muchas maneras. Esto implica la realización de una serie de pruebas básicas utilizando, por ejemplo, papeles de prueba de pH (como el papel de tornasol) y productos químicos (como los indicadores universales), o bien elementos de equipo más sofisticados como colorímetros, fotómetros y sensores electroquímicos.
Desarrollo de una ruta de trabajo dependiente de datos para la selección de péptidos para detección robusta de maní en especias
Determinación de pesticidas polares en uvas utilizando un sistema compacto de cromatografía iónica acoplado en tándem a un espectrómetro de Masas
Determinación rápida de componentes bromados en bebidas carbonatadas usando combustión oxidativa pirolítica y cromatografía iónica
Aplicaciones del nuevo Software Chromeleon 7.3.1 de Thermo Fisher Scientific
Capacitación básica en Cromatografía Iónica - módulo fundamentos de Cromatografía Iónica + deteccion por conductividad
Webinar on Demand -Determinación de dimetilamina y nitrito en productos farmacéuticos mediante IC